Índice de Saturación de Langelier.
Para evitar problemas en su manejo y tratamiento, lo ideal es que un agua sea equilibrada. El Índice de Saturación de Langelier es una medida de la estabilidad de la alcalinidad del agua potable. Un índice de saturación de Langelier positivo indica que el agua está sobresaturada con respecto a los carbonatos y, por lo tanto, es más alcalina. Por otro lado, un índice negativo indica que el agua está sub-saturada y es más ácida. Un índice de saturación de Langelier cercano a cero indica que el agua está en equilibrio y es neutra. La optimización del índice de saturación de Langelier en agua potable es importante para garantizar la calidad y evitar problemas en tuberías o equipos domésticos e industriales.
Un agua corrosiva, afecta a las tuberías y equipos de fierro.
Un agua incrustante, precipita en la mayor parte de las superficies. Algunas, como el polietileno y el polipropileno sufren menor incrustación, porque las sales que precipitan no se anclan en ellas con eficiencia.
Si un sistema no tiene partes de fierro, la corrosividad del agua deja de ser problema. Sin embargo, si un agua es incrustante, es problema en todo el sistema. Si tratamos un agua incrustante mediante los procesos típicos de potabilización, esta afecta a todos. Afecta a los filtros (de medios granulares, de cartuchos, de discos, de bolsas u otros), aunque en menor grado. Un agua incrustante:
- Precipita en las paredes del carbón activado, y este deja de realizar su función adsorbente o de eliminación de oxidantes.
- Precipita en las paredes de las resinas y estas dejan de intercambiar iones.
- Precipitan en el tubo de cuarzo de las lámparas de UV y estas dejan de desinfectar.
- Precipitan en las membranas de ósmosis inversa y las tapan.
La tendencia de un agua a ser incrustante, corrosiva o equilibrada, depende de tres parámetros:
- pH
- Alcalinidad total
- Dureza
Mientras menor es el valor de cualquiera de los tres anteriores, el agua se torna menos incrustante (o más corrosiva).
Los sólidos disueltos totales no influyen en la tendencia incrustante o corrosiva del agua, pero sí potencializan dicha tendencia, porque aumentan la conductividad del agua. Otro parámetro que potencializa la tendencia del agua es su temperatura: a mayor temperatura, la tendencia aumenta, porque la viscosidad disminuye y la movilidad de los iones (con sus respectivos electrones) aumenta.
De lo anterior, es posible disminuir la tendencia incrustante de un agua:
- Disminuyendo el pH
- Disminuyendo la alcalinidad total
- Disminuyendo la dureza total
No existe una manera exacta para calcular la tendencia incrustante o corrosiva de un agua, pero sí existen correlaciones que permiten estimar esta tendencia.
El pH se disminuye, agregando un ácido protónico.
La alcalinidad se disminuye (a) agregando un ácido; o (b) intercambiándola por otro anión (mediante resinas de intercambio iónico).
La dureza se disminuye, suavizando el agua mediante resinas de intercambio iónico ciclo sodio.
Si agregar un ácido, disminuye la tendencia incrustante de un agua, ¿por qué no simplemente hacerlo así? Hay dos razones:
- Por la peligrosidad de los ácidos fuertes, que son los más baratos y eficaces para reaccionar con la alcalinidad.
- Por lo difícil que es controlar la cantidad de ácido a agregar, para llegar al pH deseado.
Es posible reducir la tendencia corrosiva de un agua:
- Aumentando el pH
- Aumentando la alcalinidad total
- Aumentando la dureza total
El pH se aumenta, agregando un hidróxido (como sosa o potasa).
La alcalinidad se aumenta, agregando al agua un carbonato (como Calcite, que es carbonato de calcio), un bicarbonato o un hidróxido (como Corosex, que es óxido de magnesio, que al entrar en contacto con el agua se hidroliza y se disuelve como ion Mg+2 y ion OH–).
La dureza se aumenta, agregándola al agua (como puede ser a través del Calcite o el Corosex).
Índice de saturación de Langelier
Existen diversos índices con los que se estima la tendencia corrosiva o incrustante de un agua: Langelier, Ryznar, Larson y Duswell, Riddick, Mc Cauley, Caldwell-Lawrence…
Cada uno predice mejor el comportamiento del agua en determinadas condiciones.
El índice de Langelier, o índice de saturación de Langelier (ISL) es el más usado. Para un agua en particular, el ISL se calcula:
ISL = pH – pHs
En donde pH es el valor que tiene dicha agua y pHs es el valor del pH al que tendría en la saturación.
Un Índice de saturación de Langelier con un valor de cero, corresponde a un agua equilibrada. Un valor positivo corresponde a un agua incrustante y uno negativo corresponde a un agua corrosiva. Mientras el valor se aleja más de cero, mayor es la tendencia.
Es poco más que imposible tener un agua con un Índice de Langelier de cero. Puede considerarse que el agua es equilibrada cuando su valor está entre -0.3 y +0.3.
Valor del Índice de saturación de Langelier |
Tendencia del agua |
+0.3 a +2.0 |
Incrustación alta. |
0.0 a +0.3 |
Incrustación ligera con corrosión. |
0.0 |
Equilibrada. Puede ocurrir corrosión ligera. |
0.0 a -0.3 |
Corrosión ligera. No se forman incrustaciones. |
-0.3 a -2.0 |
Corrosión alta. |
El pHs depende de la alcalinidad total, la dureza total, los sólidos disueltos totales y la temperatura del agua en cuestión. Se calcula a través de gráficas, tablas o correlaciones publicadas por diversos autores. Algunas páginas en internet tienen calculadoras disponibles para hacerlo.
Corrosión Doctors publica la siguiente correlación:
pHs = 9.3 + A + B – C – D
En la que:
A = (log SDT – 1) / 10
B = 34.55 – (13.12 log T)
C = log DC – 0.4
D = log AT
En las expresiones anteriores,
SDT = concentración de sólidos disueltos totales, en mg/L
T = temperatura, en °K
DC = dureza cálcica, en mg CaCO3/L
AT = alcalinidad total, en mg CaCO3/L
Ejemplo:
¿Cuál es el valor del índice de saturación de Langelier de un agua con los siguientes parámetros: pH = 8.8, SDT = 320 mg/L, DT = DC = 150 mg CaCO3/L (toda la dureza total es cálcica), AT = 34 mg CaCO3/L y T = 25°C? ¿Qué tan corrosiva o incrustante se puede esperar que sea esta agua?
Cálculo del Índice de saturación de Langelier:
T = 25°C = 298°K
A = (log SDT – 1) / 10 = [log(320) – 1]/10 = 0.15
B = 34.55 – (13.12 log T) = 34.55 – (13.12 log 298) = 34.55 – 32.46 = 2.09
C = Log DC – 0.4 = Log(150) – 0.4 = 1.78
D = Log AT = Log(34) = 1.53
pHs = 9.3 + A + B – C – D
pHs = 9.3 + 0.15 + 2.09 – 1.78 – 1.53
pHs = 8.2
ISL = pH – pHs = 8.8 – 8.2 = 0.6
Puede preverse que esta agua sea muy incrustante.
Otro ejemplo:
Si el agua del ejemplo anterior se suaviza, ¿qué Índice de Langelier tiene ya suavizada?
Cálculos:
Al suavizar, se intercambia la dureza por sodio.
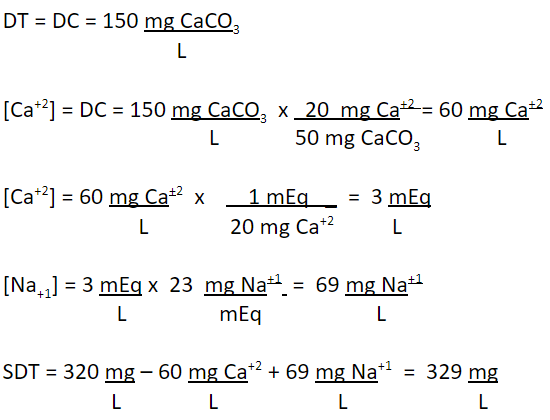
Ahora se tiene un agua con las siguientes variables:
pH = 8.8.
SDT = 329 mg/L
DT = DC = 0
AT = 34 mg CaCO3/L
T = 25°C
Cálculo del índice de Langelier:
T = 25°C = 298°K
A = (log SDT – 1) / 10 = [log(329) – 1]/10 = 0.15
B = 34.55 – (13.12 log T) = 34.55 – (13.12 log 298) = 34.55 – 32.46 = 2.09
C = Log DC – 0.4 = Log(0) – 0.4
No existe el logaritmo de cero, pero podemos suponer un valor bajo de DC. Digamos, 0.01:
C = Log DC – 0.4 = Log(0.01) – 0.4 = -2.4
D = Log AT = Log(34) = 1.53
pHs = 9.3 + A + B – C – D
pHs = 9.3 + 0.15 + 2.09 – (-2.4) – 1.53
pHs = 12.4
ISL = pH – pHs = 8.8 – 12.4 = -3.6
El agua se torna enormemente corrosiva.
Referencias.
Corrosion Doctors
(https://corrosion-doctors.org/Cooling-Water-Towers/Index-Langelier.htm)
-
RoQuest 4000 Coagulante líquido para materia orgánica Avista
Cotizar -
RoQuest 3000 Coagulante líquido orgánico de Avista
Cotizar -
Vitec 7400 de Avista para control de Sílice y Sulfatos
Cotizar -
RoClean L403 limpiador de incrustaciones por carbonato de calcio y metales de Avista
Cotizar -
RoClean P111 limpiador de membranas por bioincrustaciones
Cotizar -
RoClean P303 Limpiador de incrustaciones por carbonato de calcio y metales
Cotizar -
RoClean L211 limpieza de membranas con ensuciamiento de materia orgánica
Cotizar -
RoClean P112 Limpiador de membrana para Sílice SiO2
Cotizar

























