Cloro libre para desinfección de agua.
La cloración es el método más común para la desinfección de agua. Sin embargo, se descubrió que el cloro libre forma subproductos químicos nocivos para la salud humana. Es por esto que muchas plantas de tratamiento después de la desinfección primaria, adicionan amoniaco para convertir el cloro libre residual en cloro combinado (cloraminas). Estas también forman subproductos, aunque lo hacen en menor medida.
Química del cloro libre
La desinfección con cloro libre generalmente se logra mediante el uso de cloro gas o hipoclorito de sodio. Al inyectar cloro gas en el agua, este se disuelve y reacciona para formar ácido hipocloroso (HOCl) y ácido clorhídrico (HCl):
Cl2(g) + H2O → HOCl + HCl
Cuando se añade hipoclorito de sodio al agua, este reacciona y forma ácido hipocloroso e hidróxido de sodio:
NaOCl + H2O → HOCl + Na+ + OH–
El ácido hipocloroso (HOCl) es la especie química que aporta el mayor poder desinfectante, al ser un ácido débil este se disocia parcialmente para formar iones hipoclorito (OCl-). El grado de disociación dependerá del pH:
HOCl H+ + OCl–
El pKa para el HOCl es de 7.6 a 20°C; esto quiere decir que por debajo de este valor de pH el HOCl es la especie que se forma de manera predominante, mientras que a pH mayores predomina la formación de OCl–. Esta variable puede ser vital para la desinfección, debido a que el HOCl desinfecta de forma más rápida, por lo que es más potente que el OCl–. Si lo que se busca es reducir el consumo de cloro, se debe garantizar estar dentro del rango (4.5 – 7.0) de pH que favorece la formación de HOCl. En la figura 1, se presenta el comportamiento de las especies de cloro libre en solución acuosa, frente al pH.
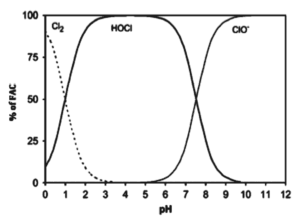
Figura 1
La desinfección con cloro se logra por medio de reacciones de oxidación que inactivan a los microorganismos presentes en el agua:
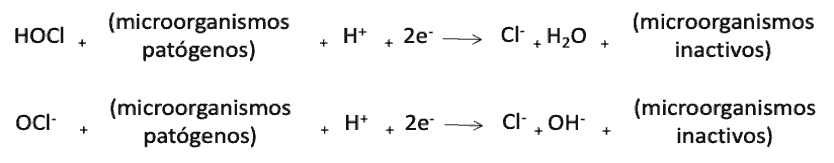
Química del cloro combinado
Cuando hay amoniaco presente en el agua, este reacciona con el cloro libre para formar especies combinadas, como cloraminas. A medida que el cloro se añade, este reacciona de forma sucesiva con el amoniaco para formar tres tipos de aminas:
NH3 + HOCl → NH2Cl + H2O (monocloramina)
NH2Cl + HOCl → NHCl2 + H2O (dicloramina)
NHCl2 + HOCl → NCl3 + H2O (tricloramina)
A la suma de la concentración de estas tres especies se le llama cloro combinado.
Las cloraminas tienen la ventaja de que no generan olores fuertes, son más efectivas en el control de películas bacterianas en tuberías y generalmente son estables. Hay que tener en cuenta que las cloraminas pueden ser consumidas por la nitrificación biológica, especialmente en temperaturas cálidas y cuando se usó amoniaco en exceso.
Demanda de cloro
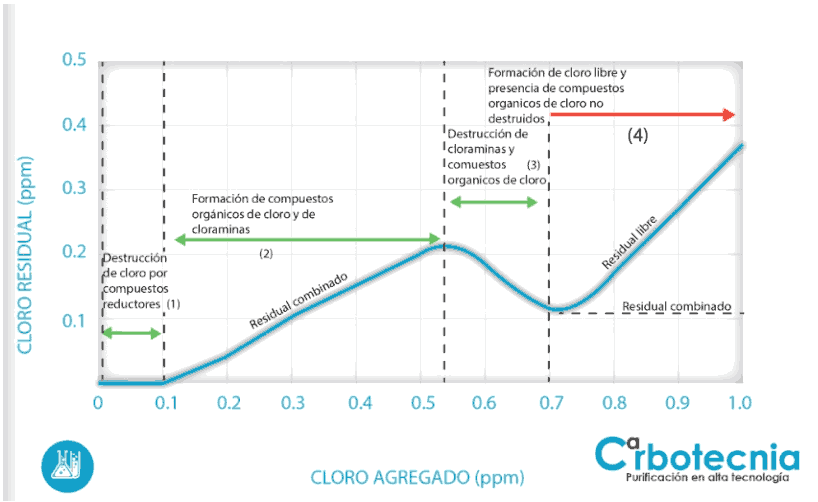
Es la cantidad de cloro que se debe añadir para: (1) reaccionar todas las sustancias fácilmente oxidables, como Fe(II), Mn(II) y H2S. Estás reacciones generalmente suceden en fracciones de segundo. (2) Al continuar con la adición de cloro este reacciona con el amoniaco y la materia orgánica presente, para formar compuestos organoclorados, como las cloraminas. Estos compuestos, también realizan una acción desinfectante, aunque de manera más lenta. (3) Si se continúa añadiendo cloro, este reaccionará con las cloraminas previamente formadas. Al punto donde termina la oxidación de las cloraminas se le llama punto de ruptura de cloro. (4) Una vez que se alcanza el punto de ruptura, el cloro que se adicione después, aumentará la concentración de cloro libre en forma directamente proporcional. En la Figura 2 se puede apreciar este proceso.
En pocas palabras, se debe adicionar el cloro suficiente para oxidar la materia orgánica e inorgánica hasta alcanzar su punto de ruptura, más la cantidad de cloro libre que se desee tener como residual de la desinfección. Para agua potable típicamente se busca estar entre 0.5 y 1.5 mg/L de cloro libre residual.
Dosis de cloro
La dosis de cloro debe ser suficiente para satisfacer la demanda de cloro y mantener un residual de cloro suficiente para inactivar o eliminar organismos patógenos. Varias propiedades físicas del agua afectan en la eficiencia de la desinfección. Una es la temperatura, ya que la viscosidad del agua disminuye al aumentar la temperatura, esto acelera el proceso de difusión. Otra es el pH, en pH menores a 7.5 obtenemos mejores resultados, debido a que aumenta la proporción de ácido hipocloroso en relación al ion hipoclorito, como ya vimos anteriormente el primero es más eficaz. La turbidez, es otro parámetro que afecta en la desinfección, debido a que los organismos patógenos se encapsulan dentro de la materia suspendida que genera la turbidez, esta capa externa los protege de la acción del cloro. Para desinfectar agua turbia de manera eficaz, es necesario aumentar la dosis de cloro, prolongar el tiempo de contacto con los patógenos, o ambas acciones.
Bibliografía
MWH’s water treatment: principles and design. John C. Crittenden et al.
BACK TO BASICS GUIDE to disinfection with chlorine. James A. Olson, 1991, AWWA.
-
AA-3 Carbón activado para reducir color y sabor en tequila y otros destilados
Cotizar -
AAM Carbón activado para eliminar color en tequila y otros destilados
Cotizar -
EBA-9 Carbón activado para tratamiento de tequilas y otros destilados
Cotizar -
IA-4 Carbón activado para tratamiento de tequilas y otros destilados
Cotizar -
Micro K Carbón activado de cáscara de coco
Cotizar -
Micro 4 LF Carbón activado de concha de coco libre de finos
Cotizar -
Megapol C – Carbón activado en polvo de madera
Cotizar -
Megapol E – Carbón activado en polvo de madera
Cotizar






















